构成生命最基本的生物大分子核酸和蛋白质具有手性均一性特征,即已知的天然核酸均由d型核糖组成,天然蛋白质几乎均由l型氨基酸组成。朱听课题组希望从镜像中心法则出发,利用化学、生物学等多学科手段构建由l型核酸和d型蛋白质组成的镜像生物学系统。到目前为止,已初步实现了镜像中心法则中的镜像核酸复制、转录、反转录等步骤,及镜像pcr、镜像核酸测序、镜像核糖核蛋白复合体组装等方法,并正在着力构建镜像蛋白质翻译系统以实现完整的镜像中心法则。
对trna进行氨基酸装载是蛋白质翻译过程的一个重要步骤。自然界中的trna氨基酸装载需要依赖一整套由数十种氨酰trna合成酶组成的复杂系统来完成。由于天然手性的氨酰trna合成酶无法识别并催化镜像trna氨基酸装载,而化学合成所有镜像版本的氨酰trna合成酶存在很大难度,因此如何找到一种适用于镜像trna氨基酸装载的方法是实现镜像蛋白质翻译必须解决的难题之一。虽然可对trna进行氨基酸装载的核酶flexizyme早在2006年就已被发现,但由于翻译效率很低,不依赖氨酰trna合成酶的蛋白质翻译一直未被实现。同时,由于传统rna化学合成技术的限制,全长镜像trna的合成效率与纯度都不高,无法被用于镜像氨基酸装载。
朱听课题组于2021年3月11日在chem杂志发表了题为“不依赖氨酰trna合成酶的蛋白质翻译”(translating protein enzymes without aminoacyl-trna synthetases)的研究论文,报道实现不依赖氨酰trna合成酶的蛋白质翻译,并尝试对镜像trna进行氨基酸装载。在该研究中,陈季等在天然手性模型中对使用flexizyme进行trna氨基酸装载的蛋白质翻译系统做了重新设计与优化,首次实现了不依赖氨酰trna合成酶的蛋白质翻译并得到多种具有活性的酶(图1)。值得一提的是,在没有氨酰trna合成酶的参与下,该系统翻译产生了具有活性的氨酰trna合成酶trprs,显示在生命起源过程中,类似具有trna氨基酸装载功能的核酶可能在蛋白质翻译系统的早期进化中发挥了重要作用。
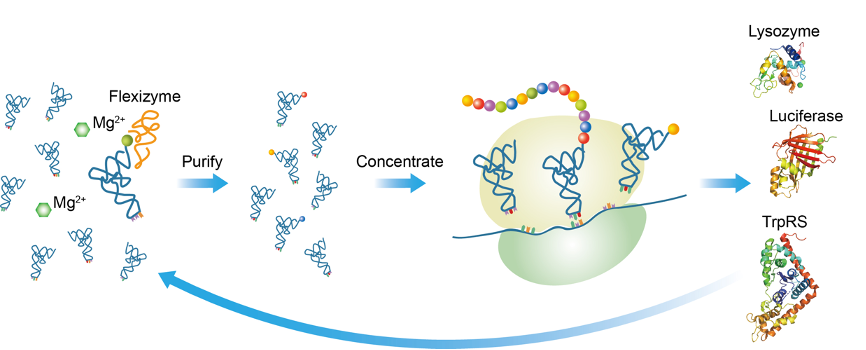
图1:不依赖氨酰trna合成酶的蛋白质翻译
在相应的镜像系统中,课题组利用优化后的镜像核酸转录方法成功制备出高纯度的全长镜像trna,并使用合成的镜像flexizyme将镜像氨基酸装载到相应的镜像trna上(图2),为将来实现镜像蛋白质翻译奠定了方法学基础。
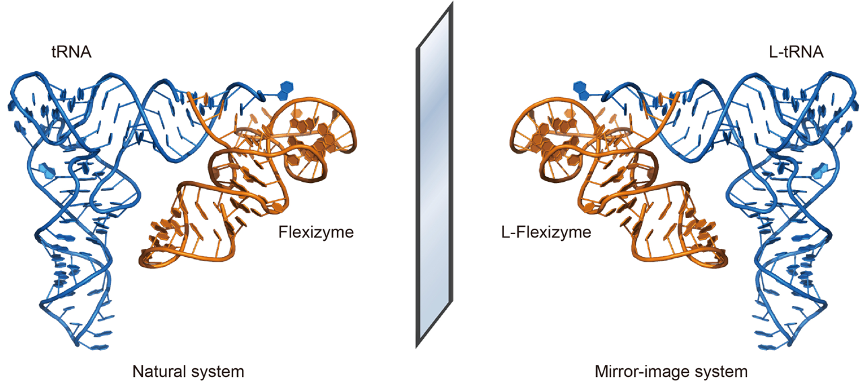
图2:使用镜像flexizyme将镜像氨基酸装载到镜像trna上
清华大学生命学院博士后、结构生物学高精尖创新中心卓越学者陈季博士为该论文第一作者,生命学院朱听教授为通讯作者。清华-北大生命科学联合中心博士生陈梦茵为该研究做出了重要贡献。该研究获得了国家自然科学基金委、清华-北大生命科学联合中心、清华大学结构生物学高精尖创新中心和北京生物结构前沿研究中心的资助。
相关论文链接: